Marco Bianchini apresenta alguns princípios sobre o papel da microbiota na doença periodontal que já são consensuais.
A interação do microbioma oral, a resposta do hospedeiro e o desenvolvimento da periodontite são complexos. A complexidade surge, em parte, da ampla gama de componentes bacterianos residentes na microbiota subgengival e das variações de indivíduo para indivíduo no repertório destas bactérias. Além disso, esta complexidade também depende das respostas imunes e inflamatórias do hospedeiro operando dentro dos tecidos gengivais. Muitas destas respostas podem ser uma forma de proteger o periodonto. Outras, porém, podem ser destrutivas, piorando ainda mais o quadro da doença. Mesmo com toda esta complexidade, alguns princípios sobre o papel da microbiota na doença periodontal já são consensuais1. São eles:
1. As bactérias são essenciais para o desenvolvimento de doenças periodontais destrutivas. Isto se comprovou através da resposta positiva ao tratamento, quando se remove o biofilme subgengival e também por experimentos em animais livres de germes, que demonstraram a necessidade de um microbioma comensal para que ocorra uma periodontite destrutiva com perda óssea1-2.
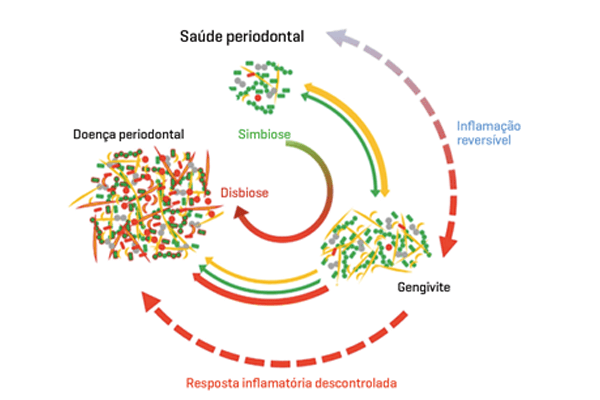
2. Mudanças na escala geral da população microbiana dos biofilmes subgengivais e na carga bacteriana destes microrganismos estão invariavelmente associadas à doença destrutiva. Estas alterações no perfil da comunidade microbiana parecem ser amplamente independentes da aquisição de novos membros da microbiota. Com isso, observa-se a predominância de organismos individuais no estado de doença ou a presença de consórcios de organismos residentes no biofilme subgengival em saúde. Essa mudança na comunidade, associada à doença ou disbiose da microbiota, pode ser impulsionada por alterações nas condições ambientais locais, onde a resposta inflamatória do hospedeiro é um provável impulsionador dessa ecologia alterada1,3.
3. Respostas inflamatórias imunes descontroladas são praticamente as responsáveis pela destruição tecidual. Com isso, estratégias terapêuticas que visam modificar estas respostas inflamatórias, que levam à destruição tecidual ou aceleram a resolução da resposta inflamatória positiva, podem fornecer uma via alternativa ao tratamento1,4.
Embora esses três princípios forneçam uma estrutura para entender o real papel da microbiota na doença periodontal, alguns pontos ainda permanecem em controvérsia. Dentro deste contexto, pode-se afirmar que as bactérias causam gengivite, pois a sua remoção leva à reversão dessa condição inflamatória. No entanto, os fatores que determinam a progressão da gengivite para periodontite, em uma proporção da população, não estão totalmente estabelecidos5. Assim, uma compreensão melhor do papel desta relação bactéria versus hospedeiro nas doenças periodontais deve ficar evidenciada, a fim de facilitar o diagnóstico e o tratamento destas doenças1.
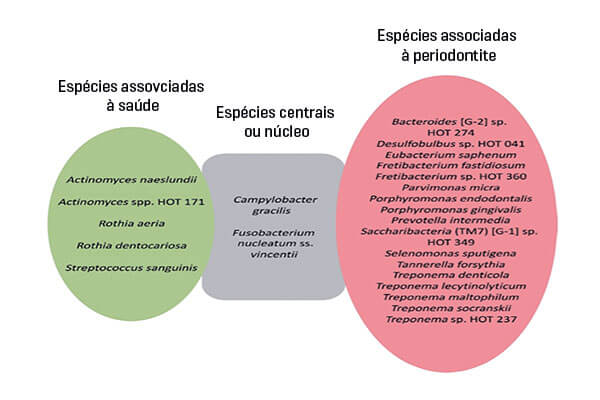
A importância da resposta do hospedeiro, através dos diferentes níveis de componentes inflamatórios produzidos, demonstra que não é totalmente verdadeiro o conceito de que a doença periodontal é uma consequência do crescimento de um número relativamente pequeno de “espécies patogênicas”, que se tornam dominantes na doença6.
A resposta inflamatória do hospedeiro e o microbioma (ataque bacteriano) estão em equilíbrio bidirecional na saúde e em desequilíbrio bidirecional na periodontite. Desta forma, uma resposta inflamatória positiva do hospedeiro, que reaja fortemente ao ataque bacteriano, pode contribuir para alterações do microbioma e com a diminuição dos fatores de virulência bacterianos, fazendo com que ocorra o arrefecimento da doença6-7.
A maioria dos indivíduos produz naturalmente respostas inflamatórias positivas ao ataque bacteriano, fazendo com que a doença não progrida. Entretanto, um grupo mais específico de pessoas não consegue modular suas respostas e a doença fatalmente avança. Assim, o tratamento ideal, que vem sendo pesquisado, seria não só a eliminação do biofilme, mas também uma ação direta no controle ativo do excesso de inflamação, a fim de modificar as respostas destes hospedeiros suscetíveis, que possa impactar positivamente no manejo da periodontite6-8.
Referências
- Curtis MA, Diaz PI, Van Dyke TE. The role of the microbiota in periodontal disease. Periodontol 2000 2020;83(1):14-25.
- Hajishengallis G, Liang S, Payne MA, Hashim A, Jotwani R, Eskan MA et al. Low‐abundance biofilm species orchestrates inflammatory periodontal disease through the commensal microbiota and complement. Cell Host Microbe 2011;10(5):497‐506.
- Marsh PD. Microbial ecology of dental plaque and its significance in health and disease. Adv Dent Res 1994;8(2):263‐71.
- Page RC, Offenbacher S, Schroeder HE, Seymour GJ, Kornman KS. Advances in the pathogenesis of periodontitis: summary of developments, clinical implications and future directions. Periodontol 2000 1997;14:216‐48.
- Vandenberg JI, Conigrave A, King GF, Kirk K. From kinetics to imaging: an NMR odyssey – a festschrift symposium in honour of Philip William Kuchel. Eur Biophys J 2013;42(1):1‐2.
- Van Dyke TE, Serhan CN. Resolution of inflammation: a new paradigm for the pathogenesis of periodontal diseases. J Dent Res 2003;82(2):82‐90.
- Hasturk H, Kantarci A, Goguet‐Surmenian E, Blackwood A, Andry C, Serhan CN et al. Resolvin E1 regulates inflammation at the cellular and tissue level and restores tissue homeostasis in vivo. J Immunol 2007;179(10):7021‐9.
- Kornman KS, Blodgett RF, Brunsvold M, Holt SC. Effects of topical applications of meclofenamic acid and ibuprofen on bone loss, subgingival microbiota and gingival PMN response in the primate Macaca fascicularis. J Periodontal Res 1990;25(5):300‐7.
Marco Bianchini
Professor associado IV do Depto. de Odontologia – Universidade Federal de Santa Catarina; Autor dos livros O Passo a Passo Cirúrgico na Implantodontia e Diagnóstico e Tratamento das Alterações Peri-implantares.