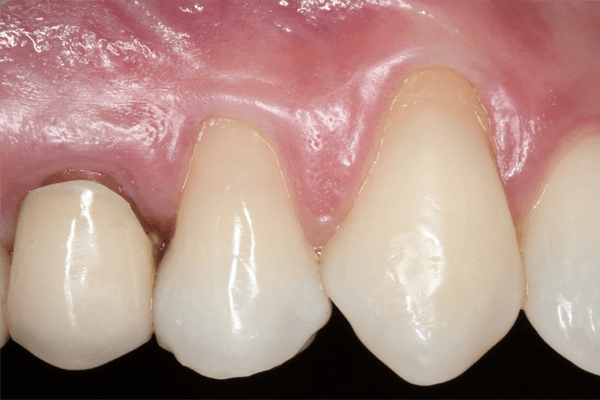
Substitutos mucosos: matéria do suplemento especial traz indicações e a evolução dos enxertos de tecido conjuntivo subepitelial autógenos.
O enxerto de tecido conjuntivo subepitelial autógeno (CTG) tem sido amplamente utilizado na Periodontia clínica nos últimos 30 anos, sendo considerado o padrão-ouro para procedimentos de aumento em volume de tecido mole periodontal e peri-implantar. As principais utilizações na cirurgia plástica periodontal e peri-implantar são em procedimentos para recobrimento radicular e peri-implantar, aumento de tecido mole em rebordos edêntulos, reconstrução de papila, aumento de tecido mole em espessura previamente à terapia ortodôntica ou para o mascaramento de raízes escurecidas e de componentes de implantes visíveis por transparência1.
Embora apresente maior previsibilidade, resultados clínicos melhores e mais estáveis em longo prazo, o uso do CTG possui algumas limitações, como quantidade limitada de tecido doador, maior duração do procedimento cirúrgico e do tempo de recuperação2, além de maior morbidade e risco de hemorragia pós-operatória devido à presença de um segundo sítio cirúrgico3. Desta forma, a busca por biomateriais que possam oferecer resultados similares ao CTG em diferentes condições clínicas tem sido o objetivo da indústria e de pesquisadores.
Diferentes biomateriais vêm sendo desenvolvidos como possíveis alternativas aos enxertos autógenos em procedimentos plásticos periodontais e peri-implantares. Atualmente, há uma variedade de substitutos mucosos disponíveis no mercado, sendo de origem alógena – por exemplo, o Alloderm (LifeCell Corp, The Woodlands – Texas, Estados Unidos) – ou de origem xenógena, dentre eles as matrizes colágenas suínas Mucograft (Geistlich Pharma AG – Wolhusen, Suíça) e Fibro-Gide (Geistlich Pharma AG – Wolhusen, Suíça), e a matriz dérmica acelular de origem suína Mucoderm (Botiss – Berlim, Alemanha). Não é factível abordarmos aqui toda a literatura relacionada à utilização de substitutos mucosos, portanto restringiremos ao uso em procedimento de recobrimentos radiculares.
A matriz dérmica acelular (ADM), como o Alloderm, é um enxerto alógeno (origem humana) caracterizado pela ausência de componentes celulares e epiteliais, sendo composto por um arcabouço de matriz conjuntiva formada por fibras colágenas tipo I/III e fibras elásticas, as quais são gradualmente degradadas e substituídas por tecidos do hospedeiro durante o período de cicatrização4. Há evidências de que a associação entre o retalho posicionado coronariamente (CAF) e o ADM para o tratamento de recessões gengivais é capaz de fornecer bons resultados clínicos. Dados de uma metanálise5 indicam taxas de frequência de recobrimento radicular completo semelhantes às obtidas com a associação CAF+CTG. No entanto, por possuir origem humana, sua comercialização é proibida no mercado nacional.
As matrizes colágenas de origem suína (CM), as quais foram desenvolvidas inicialmente para promover ganho de tecido queratinizado6, vêm sendo amplamente utilizadas em cirurgias plásticas periodontais para recobrimento radicular7-8. Apesar de o CTG ainda apresentar resultados superiores, revisões sistemáticas9-10 indicam que a associação de matrizes colágenas ao CAF para o tratamento de recessões gengivais unitárias e múltiplas é capaz de fornecer melhores resultados clínicos em termos de redução da recessão gengival e ganho em espessura de tecido marginal, quando comparada somente ao retalho. Ademais, o aumento de espessura e de altura de tecido queratinizado tem sido associado à maior estabilidade a longo prazo dos resultados obtidos e à menor recorrência das recessões gengivais11. Em adição, as vantagens associadas da CM são: procedimentos cirúrgicos mais curtos, com menor morbidade e tempo de recuperação, e maior aceitação pelos pacientes2.
Recentemente, um novo biomaterial – o Mucoderm – vem sendo utilizado na cirurgia plástica periodontal e peri-implantar como possível alternativa aos enxertos autógenos. O Mucoderm consiste em uma matriz dérmica acelular de origem suína (XDM) e é composto por fibras colágenas tipo I/III. Sua estrutura tridimensional é semelhante ao tecido conjuntivo humano e atua como arcabouço para o crescimento e repovoamento por fibroblastos, vasos sanguíneos e epitélio dos tecidos adjacentes. Ao ser degradado e substituído ou incorporado pelos tecidos do hospedeiro, um novo tecido conjuntivo é formado12. No entanto, ainda há carência de estudos na literatura avaliando seu desempenho em longo prazo, e a maioria deles avaliou seu uso em procedimentos para o aumento de mucosa peri-implantar ou para o tratamento de recessões gengivais múltiplas. Com relação ao tratamento de recessões gengivais, estudos realizados pelo nosso grupo de pesquisa* demonstram resultados satisfatórios em termos de recobrimento radicular. Um estudo recente13, com acompanhamento longitudinal de quatro anos, demonstrou que a maior parte do recobrimento radicular ocorreu no primeiro ano de acompanhamento pós-operatório, mostrando uma redução estatisticamente significativa entre um e quatro anos de acompanhamento nas médias de recobrimento radicular e frequência de recobrimento radicular completo, bem como redução na largura da gengiva inserida. As Figuras 1 a 3 ilustram o uso do XDM (Mucoderm) para o tratamento de recessões gengivais múltiplas associadas à lesões cervicais não cariosas parcialmente restauradas com resina composta (Grandioso, VOCO GmbHe – Alemanha) e o acompanhamento pós-operatório de seis meses.
Uma nova geração de matriz colágena estável em volume – a Fibro-Gide – foi desenvolvida para o uso em procedimentos de aumento de tecidos moles14. Estudos in vitro e pré-clínicos demonstraram resultados histológicos e volumétricos favoráveis em termos de integração tecidual e ganho volumétrico15. Embora o uso desse novo biomaterial apresente um potencial promissor, as evidências clínicas disponíveis ainda são limitadas e provenientes, principalmente, de estudos que avaliaram o seu desempenho em procedimentos para aumento de tecido mole peri-implantar. Há apenas um estudo clínico-piloto avaliando o uso para tratamento de recessões gengivais unitárias16.
Apesar de apresentarem custo mais elevado, as principais vantagens dos substitutos mucosos consistem na eliminação do segundo sítio cirúrgico, reduzindo, consequentemente, a duração do procedimento cirúrgico e a morbidade pós-operatória. Por conseguinte, as principais indicações clínicas de matrizes colágenas em procedimentos para recobrimento radicular são: a) presença de contraindicação para a remoção de enxerto do palato devido à disponibilidade limitada de tecido doador ou condições sistêmicas preexistentes2; b) casos em que tanto o paciente quanto o clínico buscam limitar a morbidade associada ao procedimento cirúrgico e estão dispostos a aceitar resultados clínicos potencialmente inferiores aos fornecidos pelo padrão-ouro (CTG)2.
Outro aspecto importante em relação à indicação desses biomateriais seria utilizar as matrizes nos casos adequados. Como mencionado anteriormente, a presença de uma faixa de tecido queratinizado e a espessura do tecido gengival, são fatores importantes para o recobrimento e para a manutenção dos resultados em longo prazo. Portanto, no caso de recessões RT1 de Cairo17 sem presença de tecido queratinizado, apesar de ser um tema ainda controverso, seria prudente utilizar CTG associado ao CAF. Dessa forma, matrizes podem ser empregadas nos casos onde há uma faixa de tecido queratinizado igual ou maior a 2 mm. Adicionalmente, segundo autores18, recessões que atingem 1,4 mm de espessura de tecido marginal no pós-operatório têm mais chances de obter recobrimento radicular completo. Como a literatura aponta, o ganho em espessura promovido pelas matrizes colágenas fica ao redor de 0,3 mm a 0,5 mm. Dessa forma, áreas de recessões com tecidos extremamente finos (< 0,8 mm) devem ser tratadas com CTG, e as matrizes devem ser aplicadas em locais onde o tecido gengival já tem uma espessura maior que 0,9 mm.
Por fim, é importante ressaltar que o sucesso clínico nos procedimentos com a utilização das matrizes e substitutos mucosos depende da sua correta indicação, técnica cirúrgica adequada e ótimos cuidados pós-operatórios.
*Ferraz FFL, Miguel MMV, Rossato A, Fonseca MB, Mathias-Santamaria IF, Santamaria MP. Effect of xenogeneic dermal matrix associated with coronally advanced flap in the treatment of single gingival recession: a case series. Journal of the International Academy of Periodontology, 2020.
Rossato A, Mathias-Santamaria IF, Ferraz LFF, Bautista CRG, Miguel MMV, Santamaria MP. Xenogeneic acellular dermal matrix for the treatment of multiple gingival recessions associated with partially restored noncarious cervical lesions: case series. Int J Periodontics Restorative Dent, 2020.
Referências
1. Zuhr O, Bäumer D, Hürzeler M. The addition of soft tissue replacement grafts in plastic periodontal and implant surgery: critical elements in design and execution. J Clin Periodontol 2014;41(15):S123-42.
2. Tonetti MS, Cortellini P, Pellegrini G, Nieri M, Bonaccini D, Allegri M et al. Xenogenic collagen matrix or autologous connective tissue graft as adjunct to coronally advanced flaps for coverage of multiple adjacent gingival recession: randomized trial assessing non-inferiority in root coverage and superiority in oral health-related quality of life. J Clin Periodontol 2018;45(1):78-88.
3. Wessel JR, Tatakis DN. Patient outcomes following subepithelial connective tissue graft and free gingival graft procedures. J Periodontol 2008;79(3):425-30.
4. Scarano A, Barros RR, Iezzi G, Piattelli A, Novaes Jr. AB. Acellular dermal matrix graft for gingival augmentation: a preliminary clinical, histologic, and ultrastructural evaluation. J Periodontol 2009;80(2):253-9.
5. Cairo F, Pagliaro U, Nieri M. Treatment of gingival recession with coronally advanced flap procedures: a systematic review. J Clin Periodontol 2008;35(8):136-62.
6. Sanz M, Lorenzo R, Aranda JJ, Martin C, Orsini M. Clinical evaluation of a new collagen matrix (Mucograft prototype) to enhance the width of keratinized tissue in patients with fixed prosthetic restorations: a randomized prospective clinical trial. J Clin Periodontol 2009;36(10):868-76.
7. Moreira ARO, Santamaria MP, Silvério KG, Casati MZ, Nociti Junior FH, Sculean A et al. Coronally advanced flap with or without porcine collagen matrix for root coverage: a randomized clinical trial. Clin Oral Investig 2016;20(9):2539-49.
8. Sangiorgio JPM, Neves FLDS, dos Santos MR, França-Grohmann IL, Casarin RCV, Casati MZ et al. Xenogenous collagen matrix and/or enamel matrix derivative for treatment of localized gingival recessions: a randomized clinical trial. Part I: clinical outcomes. J Periodontol 2017;88(12):1309-18.
9. Cairo F, Nieri M, Pagliaro U. Efficacy of periodontal plastic surgery procedures in the treatment of localized facial gingival recessions. A systematic review. J Clin Periodontol 2014;41(15):S44-62.
10. Graziani F, Gennai S, Roldán S, Discepoli N, Buti J, Madianos et al. Efficacy of periodontal plastic procedures in the treatment of multiple gingival recessions. J Clin Periodontol 2014;41(15):S63-76.
11. Cairo F, Cortellini P, Tonetti M, Nieri M, Mervelt J, Pagavino G et al. Stability of root coverage outcomes at single maxillary gingival recession with loss of interdental attachment: 3-year extension results from a randomized, controlled, clinical trial. J Clin Periodontol 2015;42(6):575-81.
12. Pabst AM, Happe A, Callaway A, Ziebart T, Stratul SI, Ackermann M et al. In vitro and in vivo characterization of porcine acellular dermal matrix for gingival augmentation procedures. J Periodontal Res 2014;49(3):371-81.
13. Cosgarea R, Miron R, Bora R, Rosu A, Buduru S, Sculean A. Long-term results after treatment of multiple adjacent gingival recessions with the modified coronally advanced tunnel and a porcine acellular dermal matrix. Quintessence Int 2020;8:2-14.
14. Thoma DS, Naenni N, Benic GI, Hämmerle CH, Jung RE. Soft tissue volume augmentation at dental implant sites using a volume stable three-dimensional collagen matrix – histological outcomes of a preclinical study. J Clin Periodontol 2017;44(2):185-94.
15. Harris RJ. Histologic evaluation of connective tissue grafts in humans. Int J Periodontics Restorative Dent 2003;23(6):575-83.
16. Stefanini M, Mounssif I, Barootchi S, Tavelli L, Wang HL, Zucchelli G. An exploratory clinical study evaluating safety and performance of a volume-stable collagen matrix with coronally advanced flap for single gingival recession treatment. Clin Oral Investig 2020;24(9):3181-91.
17. Cairo F, Nieri M, Cincinelli S, Mervelt J, Pagliaro U. The interproximal clinical attachment level to classify gingival recessions and predict root coverage outcomes: an explorative and reliability study. J Clin Periodontol 2011;38(7):661-6.
18. Rebele SF, Zuhr O, Schneider D, Jung RE, Hürzeler MB. Tunnel technique with connective tissue graft versus coronally advanced flap with enamel matrix derivative for root coverage: a RCT using 3D digital measuring methods. Part II. Volumetric studies on healing dynamics and gingival dimensions. J Clin Periodontol 2014;41(6):593-603.
19. Pini-Prato G, Franceschi D, Cairo F, Nieri M, Rotundo R. Classification of dental surface defects in areas of gingival recession. J Periodontol 2010;81(6):885-90.
20. Santamaria MP, Silveira CA, Mathias IF, Neves FLDS, dos Santos LM, Jardini MAN et al. Treatment of single maxillary gingival recession associated with non-carious cervical lesion: randomized clinical trial comparing connective tissue graft alone to graft plus partial restoration. J Clin Periodontol 2018;45(8):968-76.
Mauro Pedrine Santamaria
Especialista, mestre, doutor em Periodontia – Unicamp; Professor livre-docente da disciplina de Periodontia, chefe do Depto. de Diagnóstico e Cirurgia, professor permanente e vice-coordenador do programa de pós-graduação em Biopatologia Bucal – ICT-Unesp.
Amanda Rossato
Mestra e doutoranda na área de Periodontia pelo programa de pós-graduação em Biopatologia Bucal – ICT-Unesp.
Ingrid Fernandes
Mathias-Santamaria Mestra e doutora em Odontologia Restauradora – ICT-Unesp.